【学术动态】治疗性癌症疫苗研究获重要成果——液态金属纳米颗粒介导线粒体损伤放大ICD,协同IRE诱导特异性肿瘤免疫记忆
近日,北京中医药大学第二临床医学院(东方医院)周天主任医师团队联合中国科学院理化技术研究所饶伟研究员团队、国家纳米科学中心王磊研究员团队,在治疗性癌症疫苗与癌症免疫治疗方向取得新进展,研究论文“Liquid Metal Nanoparticles Mediated Mitochondrial Damage Enhances Immunogenic Cell Death for Cancer Vaccine Therapy”发表于Advanced Materials(中科院1区,JCR 1区,IF=26.8)。该研究提出“液态金属纳米颗粒(LMPs)+不可逆电穿孔(IRE)”的组合策略,为提升原位肿瘤免疫应答与建立长期免疫记忆提供了新的思路。

治疗性癌症疫苗的起效关键在于让机体免疫系统充分识别肿瘤抗原并形成免疫记忆,但实体瘤常受免疫抑制肿瘤微环境与抗原免疫原性不足的限制。研究团队围绕“免疫原性细胞死亡(ICD)”这一关键过程,设计构建了可靶向肿瘤细胞的液态金属纳米颗粒:颗粒进入细胞后持续释放Ga3+,干扰线粒体正常代谢过程并放大线粒体损伤,从而增强ICD相关危险信号与免疫激活通路,为后续抗原呈递与T细胞应答奠定基础。
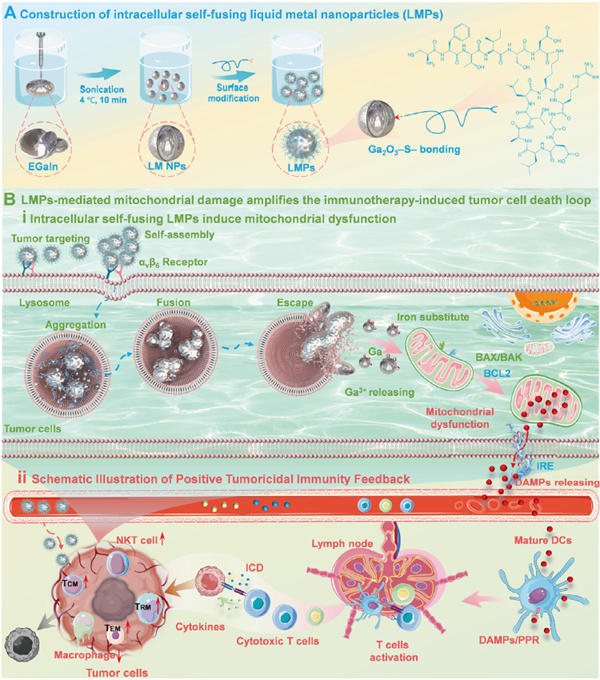
本研究创造性的解决了纳米递送体系长期存在的“尺寸两难”问题——小颗粒易进入但不易久留,大颗粒易久留但难进入。研究者利用液态金属材料特性与肽修饰设计,使LMPs在肿瘤细胞表面受体介导下增强摄取,进入溶酶体后在酸性/酶环境中发生自融合,实现“先小后大”的胞内尺寸跃迁,形成更持久的细胞内滞留与持续释放库,为实现持续线粒体应激与ICD放大提供了结构与物质基础。
在动物实验中,团队进一步将“生化启动”与“物理触发”进行时序耦合:LMPs瘤内注射后在肿瘤局部表现出更强滞留(96小时肿瘤区信号强于对照组),并据此选择注射后48小时实施IRE,以促进DAMPs与肿瘤抗原更充分释放与免疫可及性提升。治疗结果显示,联合方案显著增强肿瘤控制与长期生存获益;同时肿瘤组织可观察到与抗肿瘤免疫相关的细胞浸润增强。
更重要的是,研究通过再挑战实验验证了“肿瘤特异性免疫记忆”的建立:联合治疗可诱导更强的肿瘤特异性T细胞反应,并在同源肿瘤再接种中获得显著保护;而对异源肿瘤并未表现出同等保护,提示该记忆应答具有抗原特异性。
本研究得到国家自然科学基金面上项目等支持。戚瑜瑕、于中阳、张杰三位博士为共同第一作者,周天、王磊、饶伟为共同通讯作者。本研究面向实体瘤“局部治疗后复发与免疫应答不足”等临床痛点,再次验证了“两步法”肿瘤原位疫苗策略及其协同抗癌方案的可行性和优势性,是本团队在治疗性癌症疫苗方向新的里程碑式突破。该成果的突破,既是多学科交叉融合的成功实践,也彰显了北京中医药大学第二临床医学院(东方医院)在科研领域“立足临床、瞄准前沿、协同创新”的鲜明导向。
未来,北京中医药大学第二临床医学院(东方医院)将持续聚焦中西医融合防治重大疾病的核心关键问题,深化与顶尖科研机构的合作联动,加速推动更多基础研究成果向临床应用转化,为提升我国肿瘤诊疗水平、守护人民群众生命健康贡献东方力量。
文图/戚瑜瑕 张可睿
编辑/周丹袂
审阅/郭翔宇 曹俊岭






 京公网安备11010602050067
京公网安备11010602050067